Ré-examen du lien entre l'utilisation de l'e-cigarette et l'infarctus du myocarde : un conte édifiant


Une nouvelle contre étude démontre l'absence de corrélation entre cigarette électronique et infarctus du myocarde ; nous l'avons traduite pour vous.
Contexte
Des analyses transversales ont suggéré que l'utilisation de l'e-cigarette, indépendamment de l'utilisation de la cigarette combustible, augmente le risque d'infarctus du myocarde. Les chercheurs précédents ont confondu les hypothèses de leurs propres modèles selon lesquelles ces risques étaient indépendants avec l'idée que leurs analyses validaient la présence de risques indépendants. Cette étude évite ce piège.
Méthodes
Des analyses transversales des enquêtes nationales sur la santé 2014-2019 (N=175 546) ont été réalisées en 2020.
Résultats
Des régressions logistiques ont montré que l'utilisation de l'e-cigarette était associée à la survenue d'un infarctus du myocarde, mais que cette association variait significativement en fonction des antécédents de tabagisme. Après contrôle d'une série de variables démographiques et cliniques, l'utilisation de l'e-cigarette n'était associée à la survenue d'un infarctus du myocarde au cours de la vie que chez les fumeurs actuels. Une analyse contrefactuelle a d'abord éliminé tous les répondants (actuels ou anciens) utilisant l'e-cigarette qui avaient subi un infarctus du myocarde sans antécédents de tabagisme. Le modèle à effets indépendants utilisé dans les recherches précédentes indiquait à tort que le vapotage quotidien augmentait de 1,55 (IC 95 % = 1,11, 2,15) la probabilité d'avoir subi un infarctus du myocarde chez les personnes n'ayant jamais fumé, alors qu'il ne restait aucune victime, non fumeuse, d'infarctus du myocarde dans les données analysées. L'association entre l'infarctus du myocarde et le fait de fumer quotidiennement a montré une baisse annuelle significative (AOR=0,81, IC 95%=0,67, 0,98).
Conclusions
Il n'y a pas de preuve fiable que l'utilisation de l'e-cigarette soit associée au fait d'avoir déjà eu un infarctus du myocarde chez les personnes n'ayant jamais fumé. Contrairement aux inquiétudes selon lesquelles les méfaits associés aux e-cigarettes n'apparaissent que maintenant, après un plus grand nombre d'années d'utilisation possible du produit, les seules preuves d'une variation dans le temps de l'association entre l'utilisation des e-cigarettes et l'infarctus du myocarde vont à l'encontre de cette possibilité. La communauté scientifique doit insister pour que les chercheurs s'engagent dans une communication publique honnête des résultats évalués par leurs pairs.
Introduction
Les e-cigarettes ont été présentées comme des outils efficaces pour le sevrage tabagique. Les analyses transversales et les ECR montrent que les e-cigarettes sont des outils de sevrage tabagique et conduisent à des résultats supérieurs en la matière. Cela dit, les organismes de santé publique et les décideurs politiques ne sont pas tous d'accord avec l'adoption ou la résistance de ces produits, en partie à cause des incertitudes quant aux conséquences d'une utilisation prolongée.
Bien que les e-cigarettes soient largement considérées comme plus sûres que les cigarettes à base de tabac combustible, certains ont affirmé que le vapotage augmente le risque de divers événements de santé négatifs, notamment l'infarctus du myocarde (IM). Il est essentiel de mieux comprendre si le vapotage présente effectivement des risques pour la santé cardiovasculaire afin de formuler et d'évaluer les politiques publiques et d'étayer les recommandations cliniques.
Il est important de noter que ces recherches ont été transversales et qu'elles ont mis en évidence une association significative entre le fait d'avoir déjà subi un infarctus et le fait d'être un utilisateur actuel d'e-cigarettes. En outre, les recherches précédentes n'ont pas testé de manière exhaustive si l'association varie en fonction des antécédents de tabagisme. Mais au moins trois raisons le suggèrent. Deux d'entre elles considèrent que les e-cigarettes n’ont pas de rôle causal dans l'apparition des infarctus.
Premièrement, l'utilisation de l'e-cigarette peut être une conséquence et non une cause de l'IM. Les simulations montrent que seule une petite minorité de fumeurs de cigarettes souffrant d'infarctus adoptant les e-cigarettes suffirait à reproduire le lien entre le vapotage et l'infarctus. De plus, une nouvelle analyse de l'un des ensembles de données a révélé que pour obtenir des résultats significatifs il a été nécessaire d'ignorer le fait que bon nombre de vapoteurs ayant subi un infarctus du myocarde ont commencé à vaper après avoir subi un infarctus.
Deuxièmement, l'utilisation de l'e-cigarette peut simplement permettre d'identifier les fumeurs les plus exposés aux maladies liées au tabagisme. Les fumeurs qui adoptent les e-cigarettes peuvent avoir utilisé des cigarettes combustibles avec plus de fréquence et d'intensité ou peuvent avoir adopté les e-cigarettes parce qu'ils ont commencé à avoir des problèmes de santé. Par exemple, les fumeurs chez qui on a diagnostiqué une maladie respiratoire sont plus susceptibles de commencer à utiliser l'e-cigarette par la suite.
Troisièmement, les e-cigarettes pourraient être plus nocives pour les fumeurs actuels que pour les non-fumeurs. Ces preuves sont mitigées. Dans une étude, les fumeurs - contrairement aux non-fumeurs - ont ressenti les mêmes effets aigus négatifs sur la fonction plaquettaire après un seul vapotage qu'après un seul épisode de tabagisme. Mais lors d'une expérience ultérieure, les fumeurs de cigarettes qui sont passés à l'e-cigarette ont constaté une amélioration significative de la fonction endothéliale et de la rigidité vasculaire.
Pour renforcer la plausibilité que le lien entre l'e-cigarette et l'infarctus du myocarde pourrait dépendre des antécédents de tabagisme, on a constaté que l'utilisation de l'e-cigarette était associée aux maladies cardiovasculaires et aux attaques cardiaques chez les fumeurs mais pas chez les non-fumeurs.
Traiter le tabagisme comme une variable confusionnelle - l'approche adoptée par les études précédentes du lien entre l'IM et le tabagisme - plutôt que comme un modificateur d'effet ne résout pas ce problème et peut entraîner des résultats trompeurs. La présente recherche montre que le fait de ne pas tenir compte de cette modification de l'effet constitue une faille critique.
Études transversales antérieures établissant un lien entre l'infarctus du myocarde et l'utilisation de l'e-cigarette
En analysant les enquêtes de la « National Health Interview Survey » (NHIS) de 2014 et 2016, Alzahrani et al. a étudié les liens entre le fait d'avoir déjà subi un infarctus et l'utilisation de cigarettes combustibles et d'e-cigarettes, modélisées comme deux facteurs de risque indépendants. Après contrôle d'un grand nombre de variables démographiques et sanitaires, les fumeurs et anciens fumeurs ainsi que les vapoteurs quotidiens étaient tous plus susceptibles d'avoir déjà subi un infarctus.
Alzahrani et ses collègues soulignent à juste titre que leurs modèles testent et démontrent donc des effets statistiquement indépendants du tabagisme et du vapotage, mais si le vapotage et le tabagisme ne sont pas en fait des contributeurs indépendants à l'identification de l'occurrence de l'infarctus - c'est-à-dire si l'association entre l'utilisation de l'e-cigarette et l'occurrence de l'infarctus varie en fonction de l'utilisation de la cigarette combustible - alors le modèle à effets principaux ne peut pas être utilisé pour tirer des conclusions sur l'association entre l'utilisation de l'e-cigarette et l'infarctus, indépendamment de (ou sans) l'historique de l'utilisation de la cigarette combustible.
Ces chercheurs ont également affirmé que leur approche tenait compte de la causalité inverse : "Si quelqu'un passait de la cigarette à l'e-cigarette pour arrêter de fumer après un infarctus et que le risque accru était dû au fait d'être un ancien fumeur, ce risque serait pris en compte dans la variable de l'ancien fumeur plutôt que d'apparaître comme un artefact dans l'une des variables de l'e-cigarette " (p. 459).
Cependant, les anciens fumeurs constituent un groupe hétérogène qui comprend ceux qui fumaient occasionnellement pendant leur adolescence et ceux qui avaient l'habitude de fumer un paquet par jour pendant des décennies. Dans la mesure où les personnes appartenant au premier groupe sont moins susceptibles d'avoir subi un infarctus et d'avoir adopté l'e-cigarette, la causalité inverse n'est pas prise en compte par le modèle à effets indépendants.
Enfin, Alzahrani et al. reconnaissent que certains des infarctus peuvent s'être produits avant l'introduction des e-cigarettes, mais affirment que cela "biaisera les estimations de l'OR [du vapotage sur le risque d'infarctus] vers la valeur nulle" (p. 459). La validité de cette déclaration dépend du fait que l'initiation à l'e-cigarette n'est pas plus importante - toutes choses égales par ailleurs - chez les personnes ayant déjà subi un infarctus que chez les autres.
Bhatta et Glantz 6 ont reproduit l'association entre le vapotage et l'infarctus du myocarde lors de la première vague d'un ensemble de données longitudinales. En outre, ces auteurs ont examiné les fumeurs quotidiens ou actuels de la première vague qui ne vapotaient pas. Parmi ces sous-ensembles de répondants, ceux qui avaient eu un infarctus avant la première vague n'étaient pas plus susceptibles (que ceux qui n'en avaient pas eu) d'être passés aux e-cigarettes lors de la deuxième vague. Ils en concluent que "la causalité inverse ne peut pas expliquer l'association transversale entre l'utilisation de l'e-cigarette et l'infarctus". (Résumé). Mais considérez qui sont ces fumeurs : ce sont des personnes qui ont déjà souffert d'un infarctus et qui ont choisi de continuer à fumer. En d'autres termes, ils sont sélectionnés dans cette analyse précisément parce qu'ils ont fait preuve d'un engagement particulièrement fort envers l'utilisation de la cigarette combustible. Il n'est pas surprenant que ces fumeurs persistants ne soient pas plus susceptibles de passer au vapotage que ceux dont l'engagement à fumer n'a pas été testé de la même manière.
En fait, une autre analyse de cet ensemble de données a révélé que le fait de subir un nouvel infarctus entre ces deux vagues était associé à une augmentation de 40 % de la probabilité d'arrêter le tabac avec combustion (IC 95 % = -20, 160) et de 70 % de la probabilité d'ajouter un produit sans combustion (IC 95 % = -20, 270). De telles estimations ponctuelles suggèrent que le lien entre l'infarctus du myocarde et le tabagisme peut être attribuable à une causalité inverse ; la largeur des IC témoigne du petit nombre de répondants qui ont subi un nouvel infarctus du myocarde. Les analyses transversales focales qui montrent des relations entre l'utilisation de l'e-cigarette et le fait d'avoir déjà eu un infarctus (et pas seulement au cours des derniers mois) ne souffrent pas des mêmes limitations de puissance statistique.
Enfin, 2 autres aspects des analyses de Bhatta et Glantz remettent en question le fait que le vapotage provoque des infarctus.
Premièrement, alors que le tabagisme au cours de la première vague prédisait une nouvelle incidence d'infarctus au cours de la deuxième vague, l'utilisation de l'e-cigarette ne le faisait pas.
Deuxièmement, l'utilisation de l'e-cigarette lors de la première vague n'a été associée de manière significative à l'apparition d'un infarctus que parce que les chercheurs ont inclus les infarctus qui se sont produits avant que le vapotage ait pu les provoquer.
Cette expression de préoccupation a conduit à l'article de Bhatta et Glantz 6 en cours de rétractation par les rédacteurs du Journal de l'American Heart Association. Cela dit, d'autres détails de cet article - y compris un raisonnement statistique inapproprié - restent tout à fait pertinents pour évaluer les preuves existantes selon lesquelles l'utilisation de l'e-cigarette peut être un facteur de risqueindépendant d'infarctus.
Les présentes analyses
Sur le plan empirique, ce document s'appuie sur les efforts précédents de trois manières.
Premièrement, alors que Alzahrani et al. a analysé les données des enquêtes NHIS de 2014 et 2016, les présentes analyses incluent également les données des enquêtes de 2015 et 2017-2019.
Deuxièmement, cette enquête teste si l'association entre l'utilisation de l'e-cigarette et l'IM dépend de l'utilisation actuelle ou passée de cigarettes combustibles.
Troisièmement, ce travail teste des modèles supplémentaires pour examiner si la relation entre le vapotage et l'IM s'est accrue au fil du temps. Si l'association transversale émerge parce que le vapotage provoque un infarctus, on pourrait s'attendre à ce que ces associations se développent (une fois qu'il y aura eu plus de temps pour que les e-cigarettes, une catégorie de produits relativement nouvelle, aient réellement un impact sur la santé cardiaque).
Plus important encore, ce document présente une mise en garde qui identifie les défauts qui sont apparus dans l'enquête et l'interprétation des ensembles de données connexes.
Ces erreurs ont pris deux formes :
D'une part, on n'a pas compris que les résultats d'un modèle peuvent en révéler davantage sur les hypothèses qu'il contient que sur les associations potentiellement significatives dans les données analysées.
Un deuxième problème concerne la pratique consistant à tirer et à diffuser des conclusions causales à partir de données corrélationnelles. Dans certains cas, cela peut refléter une sous-appréciation de ce que sont réellement les extrapolations fondées sur une inférence causale.
En même temps, cette étude montre comment les données transversales peuvent être explorées pour tester les résidus empiriques qui donnent plus de plausibilité à certains facteurs causaux qu'à d'autres. Cela dit, ces efforts doivent être entrepris en étant pleinement conscient que ces analyses nuancées restent corrélationnelles et ne peuvent donc pas traiter définitivement de la causalité.
Méthodes
Population étudiée
Administré par le Census Bureau, le NHIS est livré à un échantillon aléatoire d'adultes américains. Ces analyses ont utilisé les enquêtes 2014-2019.
Mesures
Les analyses, réalisées en 2020 dans SPSS, version 27, ont inclus les répondants (N=175 546) pour lesquels le NHIS a offert des réponses complètes et valides pour les variables énumérées dans le tableau 1. Ces variables étaient celles utilisées par Alzahrani et ses collègues 5 dans leur analyse de deux ans de ces données.
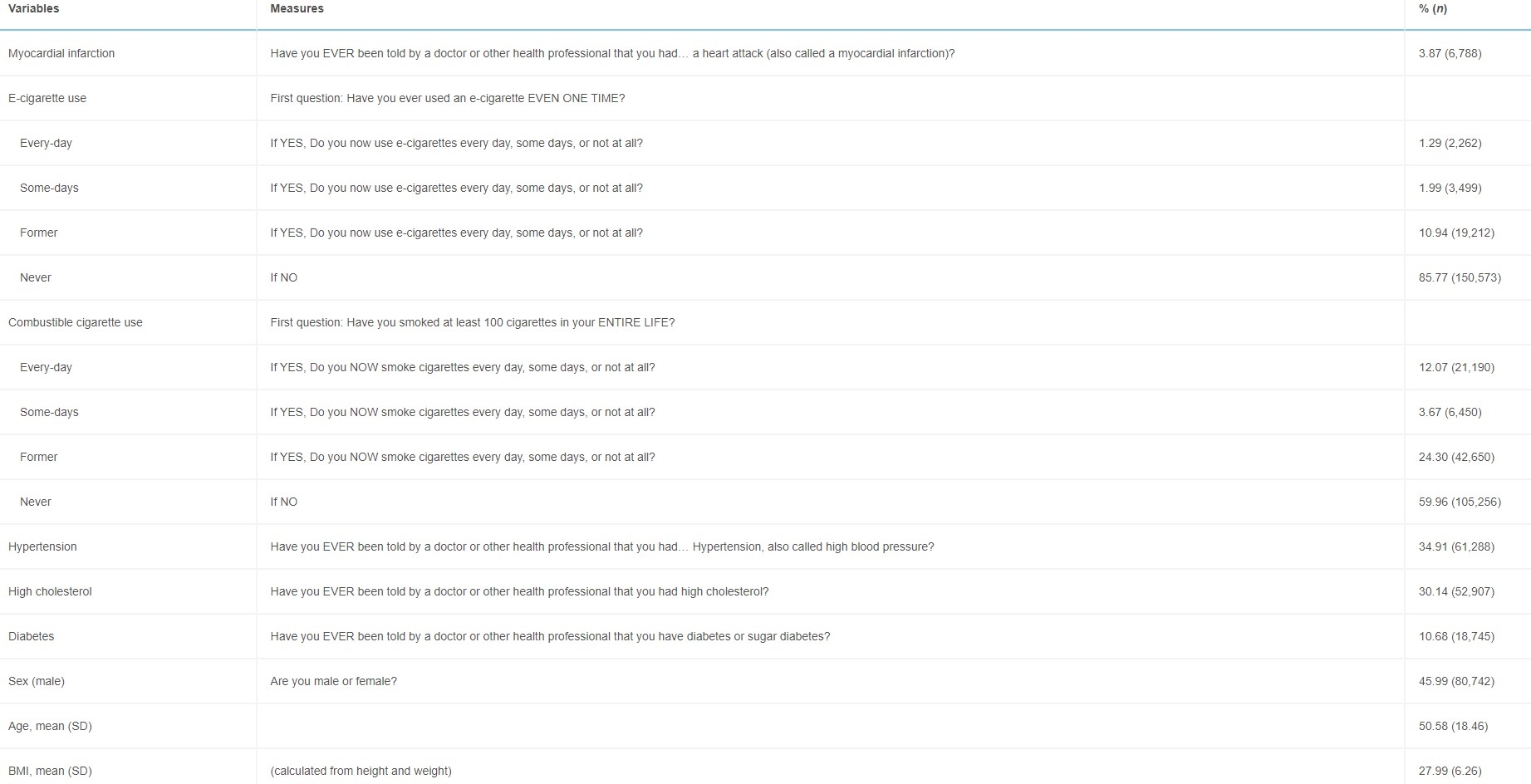
Tableau 1 : Mesures et caractéristiques de l'échantillon brut (non pondéré)
Variables Mesures % (n) Infarctus du myocarde
Remarque : pour correspondre à Alzahrani et al. (2018), les personnes qui ont répondu à la question sur le diabète en répondant à la limite ont été codées comme n'ayant pas de diabète. Pour l'âge et l'IMC, la dernière colonne affiche la moyenne et l'écart-type au lieu d'un pourcentage d'échantillon et d'un compte de fréquence brut. Les statistiques descriptives par consommation de cigarettes combustibles sont fournies dans le tableau 1 de l'annexe (disponible en ligne).
Analyse statistique
Les analyses ont utilisé des régressions logistiques avec l'IM comme variable dépendante, sauf indication contraire. Ces modèles tiennent compte du plan d'enquête complexe du NHIS.
Résultats
Dans le premier modèle, l'utilisation de l'e-cigarette était le seul prédicteur (tableau 2 en annexe, disponible en ligne). Les fumeurs actuels n'étaient pas plus susceptibles d'avoir subi un infarctus (que les personnes n'ayant jamais fumé), mais les anciens fumeurs étaient moins susceptibles d'en avoir subi un (OR=0,88, IC 95 %=0,79, 0,98).
Le second modèle a ajouté la consommation de cigarettes combustibles ainsi que son interaction avec la cigarette électronique. Bien que des effets indépendants de la cigarette électronique et de la cigarette combustible aient été observés (p<0,001 pour les deux), une interaction s’est également manifestée (χ2[9]=111,12, p<0,001).
À la lumière de l’interaction qui vient d’être rapportée, la troisième série de modèles a examiné la relation entre la consommation de cigarettes électroniques et l’IM pour chaque niveau de consommation de cigarettes combustibles.
En l’absence de covariables supplémentaires, la consommation de la cigarette électronique a été associée à une incidence plus faible d’IM dans 5 des 12 groupes pertinents (tableau 2 de l’annexe, disponible en ligne).
Les associations entre l’incidence d’IM au cours de la vie et l’usage de la cigarette électronique – sans tenir compte des covariables – sont présentées simplement pour faire parallèle à l’approche initiale adoptée et faciliter ainsi une comparaison avec les analyses rapportées par les auteurs de l’étude. Alzahrani et al.5
Ces associations montrent des changements importants lors de l’introduction des covariables, 10 des 12 associations se renforçant au moins de façon directionnelle et les 5 effets protecteurs significatifs étant éliminés. De tels changements nous rappellent que les associations observées entre la consommation de cigarettes électroniques et l’IM sont très sensibles aux spécifications du modèle.
Le quatrième modèle est revenu au modèle 2, mais a ajouté toutes les covariables. Ces résultats ont permis d’établir les principaux effets de la cigarette électronique (p=0,009) et de la cigarette combustible (p<0,001) ainsi qu’une interaction entre ces deux types de cigarettes (χ2[9]=17,94, p=0,036).
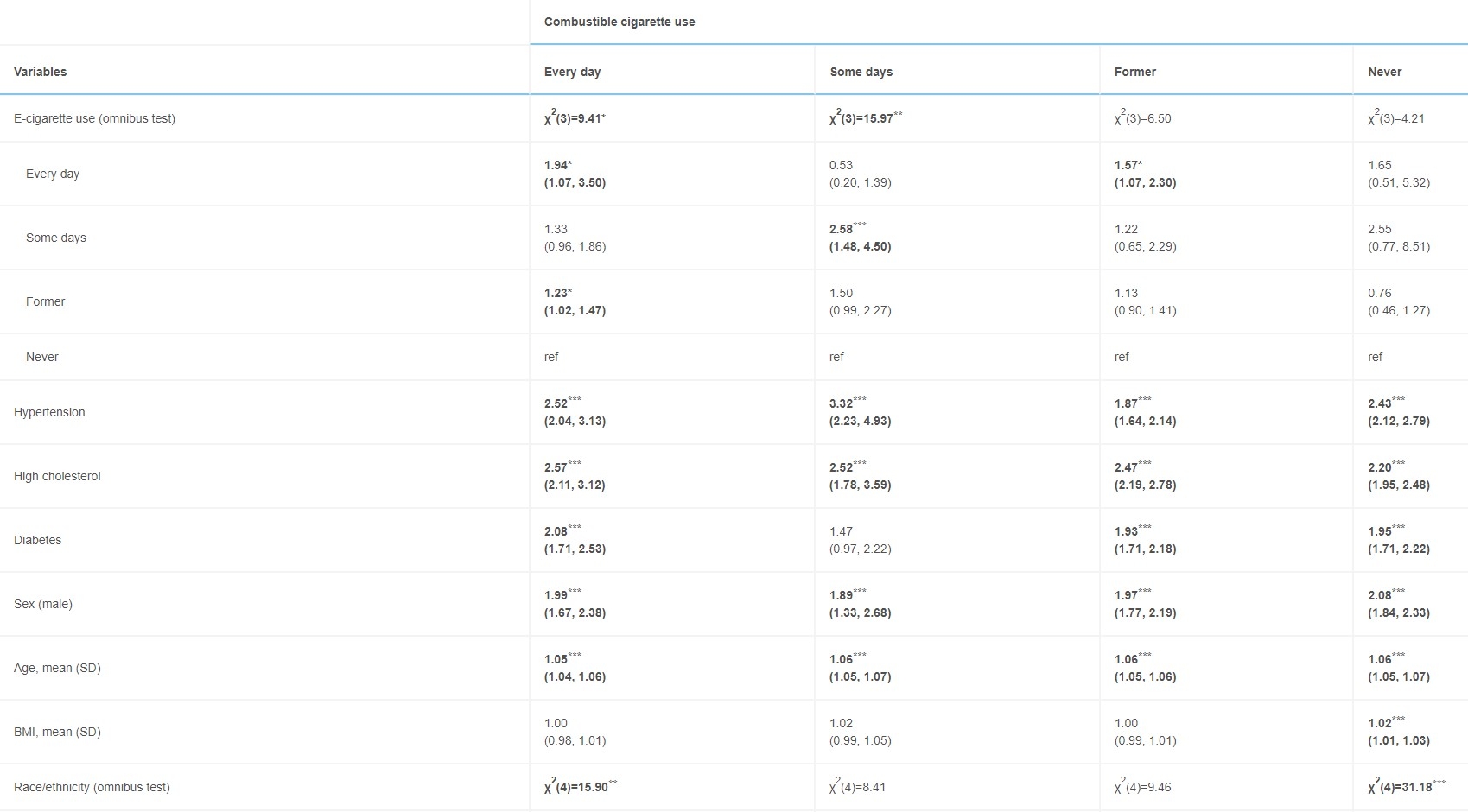
Pour interpréter l’interaction, le cinquième ensemble de modèles a examiné les associations entre la consommation de cigarettes électroniques et l’IM (contrôle des covariables) pour chacun des quatre niveaux de tabagisme. Les profils de consommation de la cigarette électronique ont été associés à l’IM chez les fumeurs quotidiens (χ2[3]=9,41, p=0,024) et certains jours (χ2[3]=15,97, p=0,001), mais non chez les anciens fumeurs (χ2[3]=6,50, p=0,090) ou n’ayant jamais fumé (χ2[3]=4,21, p=0,240) (Tableau 2).
Ces analyses ont permis de faire varier les associations avec les covariables selon le niveau de consommation de cigarettes combustibles. Cette spécification du modèle est tout à fait conforme à l’esprit de la présente étude, qui insiste sur le fait que les associations avec le MI peuvent varier selon la consommation de cigarettes combustibles. Une autre spécification, qui estimait les associations avec les covariables lors de l’effondrement de tous les niveaux de consommation de cigarettes combustibles, a donné des conclusions essentiellement similaires (tableau 3 de l’annexe, disponible en ligne).
Tableau 2 : Associations avec la survenue de l’IM au cours de la vie, selon la consommation de cigarettes combustibles (modèle 5)
Note: Les caractères gras indiquent la signification statistique (*p<0,05; t 0,01; t)
Les rangées sous l’usage de la cigarette électronique et au-dessus de la race ou de l’origine ethnique contiennent des RC ajustables (IC à 95%). Le tableau 3 de l’annexe (disponible en ligne) contient des estimations des effets de la cigarette électronique pour chaque niveau de consommation de cigarettes combustibles, sans que les estimations des covariables varient selon la consommation de cigarettes combustibles.
IM, Infarctus du myocarde.
Ouvrir la table dans un nouvel onglet
Il est possible que les cigarettes électroniques ne contribuent pas aux IM, mais les fumeurs qui ont subi un IM ou qui éprouvent déjà des effets nocifs du tabagisme sur la santé peuvent passer (ou avoir tenté) à la cigarette électronique.
Certains ont peut-être essayé la cigarette électronique avant de retourner au tabagisme quotidien (ancien vapoteur/fumeur de tous les jours).
D’autres sont peut-être devenus des utilisateurs doubles – utilisant les deux produits quotidiennement (vapoteur de tous les jours/fumeur de tous les jours) ou en alternant entre les deux produits (fumeur certains jours/vapoteur certains jours) – dans le but de réduire la consommation de cigarettes combustibles.
Certains peuvent remplacer entièrement les cigarettes par des e-cigarettes (vaper quotidien/ancien fumeur).
Ces quatre groupes étaient les seuls pour lesquels l’usage de la cigarette électronique était systématiquement associé à un IM. Si les données du NHIS avaient déterminé le moment des IM en ce qui concerne le déclenchement de la cigarette électronique, cela aurait également aidé à évaluer la plausibilité de la causalité inverse. (MI encourage l’initiation à la cigarette électronique) mais pas celle de la troisième variable causalité (la détérioration de la santé liée au tabagisme peut encourager l’initiation à la cigarette électronique et prédire l’IM).
Selon une autre possibilité, ces données indiquent que les cigarettes électroniques contribuent de façon causale aux IM subséquentes, mais la relative nouveauté de la catégorie des produits de la vape signifie que les cigarettes électroniques ont eu moins de temps pour causer des IM chez les personnes qui n’avaient pas d’antécédents de tabagisme (et le déclin cardiovasculaire qui en découle).
Selon cette interprétation de l’association transversale, on pourrait s’attendre à ce que la corrélation vapotage-IM augmente de 2014 à 2019, les effets négatifs potentiels des cigarettes électroniques se manifestant plus clairement au fil du temps. Les auteurs sont revenus au modèle des effets indépendants d’Alzahrani et de ses collègues, mais ont ajouté un effet de l’année (continu) ainsi que son interaction avec la consommation de cigarettes électroniques et de cigarettes combustibles. La seule tendance séculaire significative qui s’est dégagée concernait l’incidence d’IM chez les utilisateurs quotidiens de la cigarette électronique (RCA=0,81, IC à 95%=0,67, 0,98, p=0,029).
Cela montre que l’association entre le vapotage quotidien et l’IM n’a pas augmenté, mais a diminué avec le temps. Gardez à l’esprit que peu de tendances séculaires reflètent des changements vraiment linéaires.
Le tableau 4 de l’annexe (disponible en ligne) présente les associations spécifiques entre l’IM et l’usage de la cigarette électronique et de la cigarette combustible, par année, ce qui explique la trajectoire plus précise de la tendance séculaire observée dans les données.
Il est peu probable que cela reflète une diminution du risque de la cigarette électronique. Étant donné le scepticisme croissant du public à l’égard des cigarettes électroniques. Cela pourrait être dû au fait que les fumeurs les plus à risque sont moins susceptibles de passer à la cigarette électronique. Certains de ces fumeurs cessent de fumer par d’autres moyens, tandis que d’autres continuent à utiliser des cigarettes combustibles. En effet, l’usage actuel de la cigarette électronique a diminué chez les fumeurs actuels et anciens fumeurs (comparativement à la consommation chez ceux n’ayant jamais fumé) ainsi que chez ceux qui ont (par rapport à ceux qui n’ont pas) subi un IM (p < 0,002 pour tous) (tableau 5 de l’annexe, disponible en ligne).
Bien que l’usage actuel de la cigarette électronique chez les personnes qui n’ont pas subi d’IM ait affiché une légère hausse annuelle (RCA=1,04, IC à 95%=1,01, 1,07), la consommation de la cigarette électronique chez les personnes atteintes d’IM a affiché une baisse annuelle plus marquée (RCA=0,78, IC à 95%=0,70, 0,88). Une telle baisse n’a pas été observée dans la consommation actuelle de cigarettes combustibles chez ces personnes atteintes d’IM (TA = 0,96, IC à 95% = 0,92; 1,01). Au lieu de cerner le risque croissant posé par la cigarette électronique, des recherches antérieures ont peut-être simplement contribué à façonner un discours public qui a dissuadé les fumeurs dont la santé est compromise de considérer la cigarette électronique comme un moyen de réduire les méfaits.
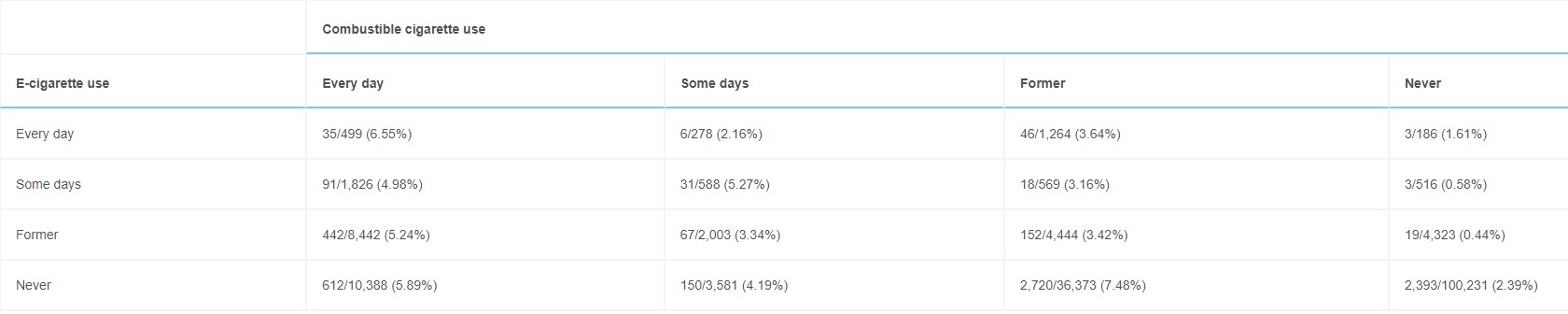
Enfin, considérons cette illustration de la façon dont les hypothèses de modélisation des chercheurs précédents ont permis de démontrer (fallacieusement) que la cigarette électronique seule est un facteur de risque d’infarctus du myocarde. Le tableau 3 montre les fréquences brutes de cas d’IM chez les utilisateurs de cigarettes électroniques dont les antécédents de tabagisme varient. Parmi les vapeurs quotidiens, 90 avaient subi un IM. Seulement 3 d’entre eux n’avaient pas fumé. Seule une de ces trois personnes – une femme de 51 ans en surpoids (IMC > 27) et ayant des antécédents d’hypertension et de cholestérol élevé – faisait partie de l’ensemble de données utilisé pour justifier la conclusion selon laquelle, pour les fumeurs de cigarettes électroniques seulement, le « risque de crise cardiaque est double pour les fumeurs quotidiens de cigarettes électroniques .» (Fernandez, communiqué de presse du 21 août 2018).
Tableau 3 : Fréquence des occurrences d’IM pour les répondants selon le type d’utilisation d’e-cigarette et de cigarette combustible
Note: Le tableau 6 de l’annexe (disponible en ligne) fournit cette information pour les répondants qui n’ont jamais fumé par année.
IM, Infarctus du myocarde
Infarctus du myocarde.
Compte tenu de la gamme des covariables utilisées, est-ce une extrapolation appropriée ? Pour comprendre pourquoi elle ne l’est pas, considérez ce qui se passe après le retrait des 25 répondants de l’ensemble de données qui ont déjà vapoté, n’ont jamais fumé et ont subi un IM. D’après le modèle à effets indépendants d’Alzahrani et coll.,5, on pourrait encore constater que même sans antécédents de tabagisme, le vapotage tous les jours (AOR=1,55, IC à 95%=1,11; 2,15), vapotage quelques jours (AOR=1,43, IC à 95%=1,11; 1,85), ou avoir déjà vapoté (AOR=1,16, IC à 95%=1,03; 1,32) augmentent significativement le risque d’avoir eu un infarctus du myocarde. Le modèle à effets indépendants par conception (mauvaise) permet de déterminer dans quelle mesure la consommation de la cigarette électronique est associée à l’incidence d’IM pour qu’elle soit équivalente dans les 4 niveaux de tabagisme.
Discussions et conclusions
L’analyse de 6 années (2014-2019) de données du NHIS a révélé que l’association entre la consommation de cigarettes électroniques et les antécédents de MI au cours de la vie dépend des antécédents de consommation de cigarettes combustibles.
Chez les personnes qui n’avaient pas d’antécédents de tabagisme, la consommation de cigarettes électroniques – passée ou présente – n’était pas associée à l’incidence d’IM. L’usage quotidien de la cigarette électronique n’a été associé à une incidence plus élevée d’IM que chez les fumeurs quotidiens et anciens fumeurs de cigarettes combustibles. Ces résultats ne concordent pas avec les conclusions d’Alzahrani et de ses collègues selon lesquelles la consommation de cigarettes électroniques seule – indépendamment de la consommation de cigarettes combustibles – est associée à l’IM. De plus, l’association entre la consommation quotidienne de la cigarette électronique et le fait d’avoir déjà eu un IM diminue. Cela pourrait refléter le scepticisme croissant des fumeurs dont la santé est dégradée à l’égard des avantages relatifs du vapotage, une possibilité appuyée par les habitudes changeantes des utilisateurs actuels de cigarettes électroniques.
La modélisation des risques comme indépendants ne permet pas d’évaluer si les risques sont indépendants
Dans une réponse publiée à Alzahrani et al.,on a fait valoir qu’il serait important d’examiner le lien entre la consommation de la cigarette électronique et l’IM chez les personnes n’ayant jamais fumé19. Deux des auteurs originaux (Alzahrani et Glantz) ont répondu que « Nous n’avons pas besoin d’effectuer ce genre d’analyse... parce que nous avons utilisé une analyse multivariable qui est ajustée pour tenir compte des facteurs confusionnels, y compris le tabagisme. » 20 Cette réponse a renforcé une affirmation qu’Alzahrani et ses collègues avaient formulée dans leur document original: « Le fait que l’utilisation des cigarettes électroniques et des cigarettes conventionnelles soit incluse dans la même régression logistique signifie qu’elles contribuent toutes deux indépendamment au risque d’avoir eu un infarctus du myocarde » (p. 457).
Ces déclarations confondent une hypothèse que les chercheurs eux-mêmes ont placée dans leur modèle (selon laquelle les cigarettes électroniques et les cigarettes conventionnelles présentent des risques indépendants) avec les conclusions que leur modèle a permis de tirer. L’usage actuel de la cigarette électronique par l’interaction de l’usage de la cigarette combustible menace la validité de cette hypothèse. Cela dit, l’argument d’Alzahrani et Glantz selon lequel le sous-ensemble des données peut « limiter considérablement la taille de l’échantillon et réduire la capacité de détecter un effet réel « (p. 569) 20 mérite une oreille attentive. Une analyse plus impartiale reconnaîtrait que, puisque les cigarettes électroniques constituent à la fois une catégorie de produits relativement nouvelle et qu’elles sont utilisées de façon disproportionnée par les fumeurs actuels et anciens, il n’est pas possible actuellement de savoir si la consommation de la cigarette électronique à elle seule entraîne (et beaucoup moins est associée de façon fiable à) un MI. S’inspirer d’un modèle à effets indépendants – qu’il s’agisse d’un modèle transversal ou d’un modèle longitudinal – ne permet pas de détecter un effet réel, mais seulement de documenter un effet mal spécifié.
Ces points incitent à une discussion plus nuancée sur le potentiel d’erreur de type I et de type II dans ce travail. Les spécifications du modèle de la présente étude se sont largement reportées aux décisions prises par Alzahrani et al. (p. ex., le choix des covariables) afin d’éviter l’adoption a posteriori des spécifications du modèle, pratique qui peut gonfler l’erreur de type I. Cela dit, l’examen d’ensembles de données indépendants qui permettent de tester les mêmes associations ou les explications proposées à leur sujet permettrait d’accroître la confiance dans la fiabilité et l’explication de certaines tendances nouvelles, comme la diminution du lien entre la consommation quotidienne de cigarettes électroniques et l’IM. Par exemple, y a-t-il d’autres données indiquant que les associations entre l’usage régulier de la cigarette électronique et l’IM (ainsi que d’autres maladies liées au tabagisme) diminuent ou augmentent à mesure que les perceptions du public à l’égard du risque de la cigarette électronique augmentent ou diminuent, respectivement ?
Le potentiel d’erreur de type II – par exemple, si l’on conclut prématurément que la consommation actuelle ou passée de la cigarette électronique n’est pas associée à une incidence plus élevée ou plus faible d’IM chez les personnes n’ayant jamais fumé – peut survenir en raison de la puissance statistique limitée. Une telle limitation peut, du moins en théorie, être corrigée en recrutant de plus grands échantillons (p. ex., des utilisateurs actuels et anciens de cigarettes électroniques qui n’ont jamais fumé). De même, même si une telle association n’existe pas aujourd’hui, cela n’exclut pas la possibilité qu’elle se forme à l’avenir. Bien sûr, une telle honnêteté épistémique sur les limites de l’observation empirique ne devrait pas être utilisée de façon rhétorique comme insinuations effrayantes. Alors que la société cherche des solutions innovantes à des problèmes de santé publique urgents (p. ex. la maladie du coronavirus 2019 [COVID-19], l’épidémie de tabagisme), il doit distinguer ce qui est actuellement inconnu de ce qui est actuellement inconnaissable. À titre d’exemple, ceux qui s’opposent à la vaccination tentent d’exploiter l’inobservation actuelle de l’avenir pour encourager l’hésitation à se faire vacciner.
La corrélation n’est pas la cause: Reconnu mais vite oublié
Les résultats actuels, qui jettent un doute sur l’interprétation selon laquelle la cigarette électronique a conduit à l’IM, soulèvent un second problème aux implications beaucoup plus vastes.
Lorsque les chercheurs font état d’analyses transversales, il est courant de reconnaître que de telles conceptions ne permettent pas de tirer des conclusions causales. Alzahrani et ses collègues suivent cette coutume: « Le NHIS est une étude transversale, de sorte qu’elle ne permet que d’identifier des associations plutôt que des relations de cause à effet. » (p. 459). Mais ensuite, les auteurs se sont appuyés sur les résultats de leur modèle pour simuler différents scénarios contrefactuels – par exemple, en demandant comment « la probabilité d’avoir eu une crise cardiaque chez une personne qui est passée de la cigarette combustible quotidiennement à la cigarette électronique quotidiennement changerait « (p. 457). Notez qu’il s’agit d’une question de causalité: Si une personne change de comportement (de la cigarette au vapotage), quelle est la probabilité qu’elle ait un MI? Par analogie, si l’on modélise la taille en fonction du poids, on ne peut alors utiliser cette donnée pour jouer des scénarios contrefactuels afin apprendre de combien un individu va rétrécir en perdant du poids.
C’est essentiellement ce qu’ont fait Alzahrani et coll., un faux pas déductif qu’ils se sont engagés à réitérer ailleurs. De plus, ils ont tiré des conclusions stratégiques de leur approche («De ces constatations [...] l’utilisation de cigarettes électroniques pour cesser de fumer ne devrait pas être recommandée», 460) 5 témoigne d’une dépendance continue à l’égard de leurs résultats comme preuve causale.
Une réponse publiée séparément, critique le manque de clarté d’Alzahrani et ses collègues qui confondent corrélation et lien de causalité en notant que leur allégation de « risque accru » laisse clairement entendre... que l’usage de la cigarette électronique précède l’IM et que l’usage de la cigarette électronique a causé l’IM « (p. 626). Alzahrani et Glantz ont répondu que «nous n’avons clairement utilisé que des termes relatifs à l’«association» pour rapporter les résultats de notre étude» (p. 627). Cette réponse est suspecte pour 2 raisons.
Tout d’abord, lorsque A est considéré comme un facteur de risque pour B, cela ne signifie pas nécessairement que A cause B, mais sans clarification, cela n’implique pas que B puisse causer A. Après tout, la malnutrition est un facteur de risque de décès prématuré. La mort prématurée n’est pas un facteur de risque de malnutrition.
Deuxièmement, (non examiné par les pairs) la communication publique des conclusions transversales des auteurs a activement favorisé l’interprétation causale selon laquelle la cigarette électronique cause l’IM (tableau 4).
Tableau 4 : Exemples de communications publiques des auteurs sur les associations transversales entre la vape et l’IM
Ils ont observé
a https://tobacco.ucsf.edu/first-evidence-long-term-health-damage-ecigs-smoking-e-cigarettes-daily-doubles-risk-heart-attacks.
b https://tobacco.ucsf.edu/risk-heart-attacks-double-daily-e-cigarette-users.
c https://tobacco.ucsf.edu/more-evidence-e-cigs-cause-heart-attacks-time-path.
d https://www.youtube.com/watch?v=iIpP_Vc9w3k. All retrieved October 14, 2020.MI, myocardial infarction; UCSF, University of California, San Francisco.
La communauté scientifique est bien consciente que les communiqués de presse, les articles de blogs et l’activisme public ne font pas l’objet d’un examen par les pairs. Cette même communauté devrait se méfier de ses membres qui parlent d’une seule voix lorsqu’ils sont soumis à examen par leurs pairs, mais qui utilisent ensuite le pouvoir de légitimation de l’examen de leurs pairs comme un titre qui les aide à diffuser leurs conclusions (fallacieuses) publiées. Des données scientifiques solides, façonnées et renforcées par un solide processus d’examen par les pairs, contribuent de façon précieuse aux politiques gouvernementales et aux recommandations cliniques. Lorsque l’intégrité de ce processus est bafouée, la légitimité des institutions collectives de la communauté scientifique est endommagée.
Remerciements
Les docteurs Leif Nelson et Yoel Inbar ont fourni des commentaires essentiels sur les premières ébauches de ce manuscrit.
Pour faciliter de plus amples analyses, les auteurs du présent document rendent public l’ensemble de données transformées et le script d’analyse utilisé dans ces analyses à l’adresse suivante: https://osf.io/4pu2m/.
Le CRC a analysé les données et a rédigé les méthodes, les résultats et la discussion. Le CRC et la MS ont rédigé l’introduction et apporté des révisions critiques à leurs textes respectifs.
Aucune information financière n’a été communiquée par les auteurs du présent document.
Appendice. MATÉRIAUX SUPPLÉMENTAIRES
Royal College of Physicians Nicotine without smoke: Tobacco harm reduction. RCP, London2016
Brose LS Brown J McNeill A. Mental health and smoking cessation-a population survey in England. BMC Med. 2020; 18: 161 https://doi.org/10.1186/s12916-020-01617-7
Hajek P Phillips-Waller A Przulj D et al. A randomized trial of e-cigarettes versus nicotine-replacement therapy. N Engl J Med. 2019; 380: 629-637 https://doi.org/10.1056/NEJMoa1808779
Abrams DB Glasser AM Villanti AC Pearson JL Rose S Niaura RS. Managing nicotine without smoke to save lives now: evidence for harm minimization. Prev Med. 2018; 117: 88-97 https://doi.org/10.1016/j.ypmed.2018.06.010
Alzahrani T Pena I Temesgen N Glantz SA. Association between electronic cigarette use and myocardial infarction. Am J Prev Med. 2018; 55 ([published correction appears in Am J Prev Med. 2019;57(4):579–584]): 455-461 https://doi.org/10.1016/j.amepre.2018.05.004
Bhatta DN Glantz SA. Electronic cigarette use and myocardial infarction among adults in the U.S. in the Population Assessment of Tobacco and Health. J Am Heart Assoc. 2019; 8 ([retracted in: J Am Heart Assoc. 2020;9(4):e014519])e012317 https://doi.org/10.1161/JAHA.119.012317
Vindhyal MR Ndunda P Munguti C Vindhyal S Okut H. Impact on cardiovascular outcomes among e-cigarette users: a review from National Health Interview Surveys. J Am Coll Cardiol. 2019; 73 (9): 11 https://doi.org/10.1016/S0735-1097(19)33773-8
Middlekauff HR Gornbein J. Association of electronic cigarette use with myocardial infarction: persistent uncertainty. Am J Prev Med. 2019; 56: 159-160 https://doi.org/10.1016/j.amepre.2018.06.007
Rodu B Plurphanswat N. A re-analysis of e-cigarette use and heart attacks in PATH wave 1 data. Addiction. 2020; 115: 2176-2179 https://doi.org/10.1111/add.15067
Bhatta DN Glantz SA. Association of e-cigarette use with respiratory disease among adults: a longitudinal analysis. Am J Prev Med. 2020; 58: 182-190 https://doi.org/10.1016/j.amepre. 2019.07.028
Nocella C Biondi-Zoccai G Sciarretta S et al. Impact of tobacco versus electronic cigarette smoking on platelet function. Am J Cardiol. 2018; 122: 1477-1481 https://doi.org/10.1016/j.amjcard.2018.07.029
George J Hussain M Vadiveloo T et al. Cardiovascular effects of switching from tobacco cigarettes to electronic cigarettes. J Am Coll Cardiol. 2019; 74: 3112-3120 https://doi.org/10.1016/j.jacc.2019.09.067
Osei AD Mirbolouk M Orimoloye OA et al. Association between e-cigarette use and cardiovascular disease among never and current combustible-cigarette smokers. Am J Med. 2019; 132 (e2): 949-954 https://doi.org/10.1016/j.amjmed.2019.02.016
Parekh T Pemmasani S Desai R. Risk of stroke with e-cigarette and combustible cigarette use in young adults. Am J Prev Med. 2020; 58: 446-452 https://doi.org/10.1016/j.amepre.2019.10.008
Greenland S Morgenstern H. Ecological bias, confounding, and effect modification. Int J Epidemiol. 1989; 18 ([published correction appears in Int J Epidemiol. 1991;20(3):824]): 269-274 https://doi.org/10.1093/ije/18.1.269
Gaalema DE Pericot-Valverde I Bunn JY et al. Tobacco use in cardiac patients: perceptions, use, and changes after a recent myocardial infarction among U.S. adults in the PATH study (2013-2015). Prev Med. 2018; 117: 76-82 https://doi.org/10.1016/j.ypmed.2018.05.004
Retraction to: electronic cigarette use and myocardial infarction among adults in the U.S. Population Assessment of Tobacco and Health [retraction of: J Am Heart Assoc. 2019;8(12):e012317]. J Am Heart Assoc. 2020; 9e014519 https://doi.org/10.1161/JAHA.119.014519
Perski O Beard E Brown J. Association between changes in harm perceptions and e-cigarette use among current tobacco smokers in England: a time series analysis. BMC Med. 2020; 18: 98 https://doi.org/10.1186/s12916-020-01565-2
Bover Manderski MT Singh B Delnevo CD. E-cigarette use and myocardial infarction: importance of a sound evidence base in the e-cigarette risks-benefits debate. Am J Prev Med. 2019; 57: 568-569 https://doi.org/10.1016/j.amepre.2019.03.012
Alzahrani T Glantz SA. Adding data from 2015 strengthens the association between e-cigarette use and myocardial infarction. Am J Prev Med. 2019; 57: 569-571 https://doi.org/10.1016/j.amepre.2019.03.008
St Helen G Eaton DL. Public health consequences of e-cigarette use. JAMA Intern Med. 2018; 178: 984-986 https://doi.org/10.1001/jamainternmed.2018.1600
Hernán MA Hsu J Healy B. A second chance to get causal inference right: a classification of data science tasks. CHANCE. 2019; 32: 42-49 https://doi.org/10.1080/09332480.2019.1579578
Alzahrani T Pena I Temesgen N Glantz SA. E-cigarettes: stick to the evidence. Am J Prev Med. 2019; 56: 160-161 https://doi.org/10.1016/j.amepre.2018.09.004
Farsalinos K Niaura R. E-cigarette use and myocardial infarction: association versus causal inference. Am J Prev Med. 2019; 56: 626-627 https://doi.org/10.1016/j.amepre.2018. 11.013
Alzahrani T Glantz SA. The association between e-cigarette use and myocardial infarction is what one would expect based on the biological and clinical evidence. Am J Prev Med. 2019; 56: 627 https://doi.org/10.1016/j.amepre.2018.11.006
Version originale, en anglais, de l'étude : https://www.ajpmonline.org/article/S0749-3797(21)00290-7/fulltext#relatedArticles

















.png)









.png)

.png)


.png)